将0.72g草酸亚铁(FeC2O4)放在一个可称量的敞口容器中高温焙烧,500~600℃时,容器中的固体质量保持0.4g不变。所得物质的化学式为( )
- A.Fe
- B.FeO
- C.Fe2O3
- D.Fe3O4
正确答案及解析
正确答案
C
解析
【分析】根据反应前后铁元素的质量不变,确定所得物质中铁元素和氧元素的质量比,进而确定其化学式。
【解答】解:0.72g草酸亚铁中含铁元素的质量为
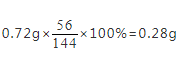
,而反应后固体质量为0.4g,不可能是铁单质,结合选项可知,应为铁的氧化物,铁元素和氧元素的质量比为0.28g:(0.4g﹣0.28g)=7:3,设铁的氧化物的化学式为FexOy,56x:16y=7:3,则x:y=2:3,故所得物质的化学式为Fe2O3。
故选:C。
【点评】本题难度不大,明确反应前后铁元素的质量不变、化学式的有关计算是正确解答本题的关键。
包含此试题的试卷
你可能感兴趣的试题
将0.72g草酸亚铁(FeC2O4)放在一个可称量的敞口容器中高温焙烧,500~600℃时,容器中的固体质量保持0.4g不变。所得物质的化学式为( )
-
- A.Fe
- B.FeO
- C.Fe2O3
- D.Fe3O4
- 查看答案
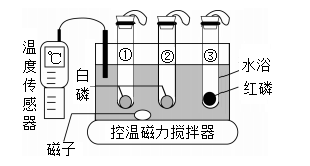
利用如图装置进行燃烧条件的探究。试管①中充满氮气,试管②③中充满氧气,升温至40℃,仅观察到②中的白磷燃烧。下列叙述错误的是( )
-
- A.由实验①②可验证燃烧需要氧气
- B.由实验②③可推知着火点高低:红磷>白磷
- C.利用水浴控温可调节可燃物的着火点
- D.①③两支试管内的白磷和红磷可回收再利用
- 查看答案
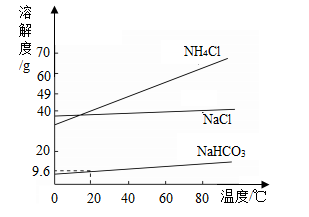
“侯氏制碱法”生产纯碱的主要反应是NaCl+NH4HCO3═NaHCO3↓+NH4Cl。如图是三种物质的溶解度曲线。下列叙述正确的是( )
-
- A.0℃时,NH4Cl的溶解度大于NaCl的溶解度
- B.20℃时,NaHCO3饱和溶液中溶质的质量分数一定大于NH4Cl不饱和溶液中溶质的质量分数
- C.20℃时,100g水中加入5.85g NaCl和7.9g NH4HCO3固体,肯定有NaHCO3晶体析出
- D.NH4Cl固体中含有少量的NaCl,可用降温结晶的方法提纯NH4Cl
- 查看答案
下列叙述正确的是( )
-
- A.
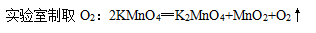
- B.工业上分离液态空气得到O2的变化属于化学变化
- C.自然界中植物通过光合作用吸收CO2,释放O2
- D.人体呼出的气体中CO2的含量比O2高
- A.
- 查看答案
如图是甲和乙在一定条件下反应前后分子种类变化的微观示意图。下列叙述正确的是( )
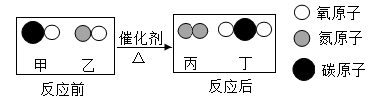
-
- A.甲与丙均属于氧化物
- B.反应生成的丙与丁的分子个数比为1:1
- C.反应后原子的数目增加
- D.该反应能使有害气体转化为无害物质
- 查看答案