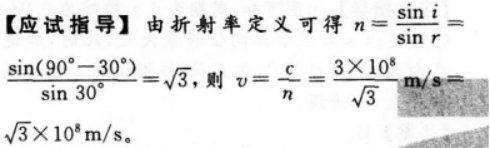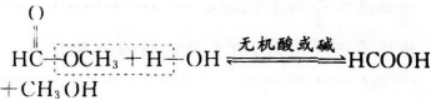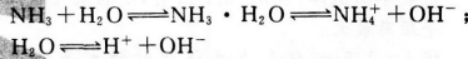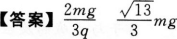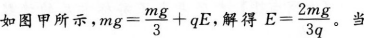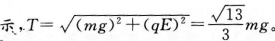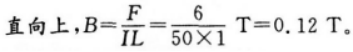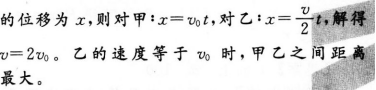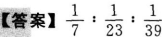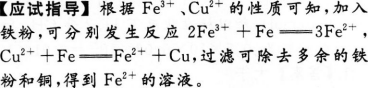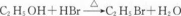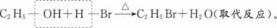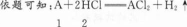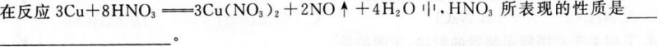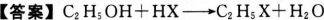下列反应的离子方程式正确的是( )。

- A 见图A
- B 见图B
- C 见图C
- D 见图D
- 参考答案:A
- 您的答案:
参考解析:
本题考查了离子方程式的知识点。

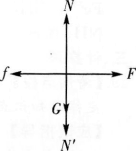
在斜面上放一物体静止不动,该物体受重力G、弹力N和静摩擦力f的作用,该物体的受力图画得正确的是( )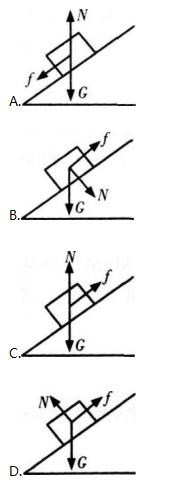
- A 见图A
- B 见图B
- C 见图C
- D 见图D
- 参考答案:D
- 您的答案:
参考解析:
本题考查了受力分析的知识点。
由弹力的性质可知,N的方向应为垂直于斜面向上。可知D正确。
关于速度和加速度的关系,下列说法正确的是( )
- A 速度变化量越大,加速度越大
- B 速度变化越快,加速度越大
- C 速度越大,加速度也越大
- D 加速度大小不断变小,速度大小也不断变小
- 参考答案:B
- 您的答案:
参考解析:
本题考查了加速度的概念的知识点。
加速度表示速度变化的快慢的物理量,故B正确。
物体在升降机中处于超重状态,关于升降机的运动状态,下列判断正确的是( )
- A 可能加速上升
- B 可能加速下降
- C 可能匀速下降
- D 可能减速上升
- 参考答案:A
- 您的答案:
参考解析:
本题考查了牛顿第二定律的知识点。
超重时,物体的加速度方向向上,故A正确。
质量为m的物体,从静止开始以2g的加速度竖直向下运动高度h,下列正确的是( )
- A 物体的重力势能减少2mgh
- B 物体的动能增加2mgh
- C 物体的机械能保持不变
- D 物体的机械能增加2mgh
- 参考答案:B
- 您的答案:
参考解析:
本题考查了功的概念的知识点。
重力加速度为9,物体下落h时,重力势能减少mgh。合力做功m·2g·h。物体的动能增加2mgh,因此,物体的机械能增加mgh-mgh=mgh,所以B正确。
抖动绳子的一端,产生如图所示的横波,则绳上横波的波长为( )
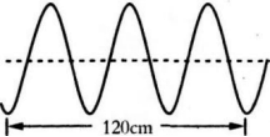
- A 120cm
- B 80cm
- C 40cm
- D 20cm
- 参考答案:C
- 您的答案:
参考解析:
本题考查了机械波的图象的知识点
由图可知3λ=120cm,得λ=40cm
下列核反应方程中,哪个方程是平衡的( )
- A 见图A
- B 见图B
- C 见图C
- D 见图D
- 参考答案:C
- 您的答案:
参考解析:
本题考查了棱反应方程的知识点
由质量数守恒、电荷数守恒可知C正确。
一定质量的理想气体经历压强增加的过程,若在此过程中( )
- A 气体的体积减小,则温度一定降低
- B 气体的体积保持不变,则温度可能不变
- C 气体的体积增大,则温度一定升高
- D 气体的体积增大,则温度可能不变
- 参考答案:C
- 您的答案:
参考解析:
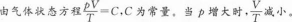
因此,当V减小时,不能确定T的变化;
当V增大时,T一定升高;当V不变时,T一定升高。所以C正确。
下列物质属于纯净物的是( )
- A 小苏打
- B “发烟”硝酸
- C 盐酸
- D 福尔马林
- 参考答案:A
- 您的答案:
参考解析:
本题考查了纯净物和混合物的区别的知识点。
纯净物和混合物的区别在于:前者只有“一种物质”组成,而后者有“多种成分”组成。B项“发烟”硝酸是浓度为98%以上的浓硝酸;C项盐酸是氯化氢气体的水溶液;D项福尔马林则是35%~40%的甲醛水溶液。这三种物质中均含有水,组成成分均不止一种,是混合物。A项小苏打(碳酸氢钠)只由“一种物质”组成,是纯净物。
下列各组中的离子,能在溶液中大量共存的是( )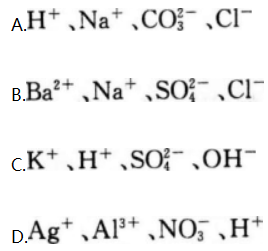
- A 见图A
- B 见图B
- C 见图C
- D 见图D
- 参考答案:D
- 您的答案:
参考解析:
本题考查了离子共存的知识点。
 OH-不能共存;D项中离子能大量共存。
OH-不能共存;D项中离子能大量共存。
把Zn粒加入0.1mol/L盐酸中,若要加快产生H,的速率,可采取的方法是( )
- A 加入少量NaOH溶液
- B 加入ZnO
- C 滴加少量CuSO4溶液
- D 滴加MgCl2溶液
- 参考答案:C
- 您的答案:
参考解析:
本题考查了影响化学反应的因素的知识点。
滴加少量CuS04溶液后,则发生反应:
下列物质在氧化还原反应中只能作还原剂的是( )
- A SO2
- B Fe2+
- C S2-
- D Na+
- 参考答案:C
- 您的答案:
参考解析:
本题考查了氧化荆与还原剂的知识点。
化学反应中失去电子或所含元素化合价升高的物质,为“还原剂”。反之,得到电子或所含元素化合价降低的物质,为“氧化剂”。A项SO2中硫元素的化合价为+4价,其化合价在化学反应中既可以升高(为+6价),也可以降低(为0价或-2价);B项Fe抖中也存在同样的情况,即SO2和Fe2+在氧化还原反应中,既可作氧化剂又可作还原剂;而D项Na+为+1价,在氧化还原反应中只能获得电子被还原,作氧化剂;C项S2-的化合价为-2价,在氧化还原反应中,其化合价只能升高,作还原剂。
下列化合物中,既含有离子键,又含有共价键的是( )
- A H2SO4
- B KCl
- C NaOH
- D CH4
- 参考答案:C
- 您的答案:
参考解析:
本题考查了离子键与共价键的知识点。
离子键:阴阳离子间通过静电作用所形成的化学键;共价键:原子间通过共用电子对所形成的化学键。本题所给选项H2SO4和CH4都是只含非金属元素,故只存在共价键。KCl中只存在离子键。NaOH中氧原子和氢原子是通过共用电子对(共价键)形成氢氧根,而Na+与OH-又通过离子键结合成离子化合物NaOH,NaOH中既有离子键又有共价键。
相同浓度的下列溶液,pH值最大的是( )
- A NH4Cl
- B NaCl
- C CH3COOH
- D NaHC03
- 参考答案:D
- 您的答案:
参考解析:
本题考查了电离、水解对pH的影响的知识点。
①CH3COOH为弱酸,其电离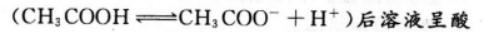 性pH<7;②NaCl为强酸强碱盐,在溶液中不水解,溶液呈中性,pH=7;③NH4Cl为弱碱强酸盐,水解后溶液呈酸性,pH<7;④NaHCO3为强碱弱酸的酸式盐,水解后溶液呈碱性,pH>7。
性pH<7;②NaCl为强酸强碱盐,在溶液中不水解,溶液呈中性,pH=7;③NH4Cl为弱碱强酸盐,水解后溶液呈酸性,pH<7;④NaHCO3为强碱弱酸的酸式盐,水解后溶液呈碱性,pH>7。
下列关于右图所示装置的叙述,正确的是( )
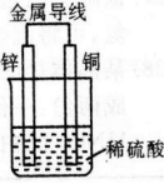
- A 铜是负极,铜片上有气泡产生
- B 该装置可以将电能转化成化学能
- C 电流从锌片经导线流向铜片
- D <img src='http://tp.mxqe.com/data/878/17359664_0_1.png' alt='物理化学综合,押题密卷,2022年成人高等考试《理化综合》(高升本)押题密卷' title='物理化学综合,押题密卷,2022年成人高等考试《理化综合》(高升本)押题密卷'>
- 参考答案:D
- 您的答案:
参考解析:
本题考查了原电池的基本原理的知识点。
如图所示装置为铜、锌原电池,其中铜作正极,铜片上有气泡产生;锌作负极,电流从铜片经导线流向锌片,发生的总反应为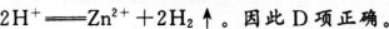
下列有关物质用途的说法错误的是( )
- A AgI可用于人工降雨
- B AgBr常用于制感光材料
- C Na2O2常用作呼吸面具和潜水艇里的供氧剂
- D BaCO3可代替BaSO4用作“钡餐”
- 参考答案:D
- 您的答案:
参考解析:
本题考查了物质的用途的知识点。
BaSO4。可用作“钡餐”,是因为既不溶于水又不溶于酸。但BaCO3虽不溶于水,但能溶于酸。其反应的离子方程式为:BaCO3+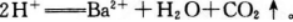
质量为M的人站在地面上,用绳通过定滑轮将质量为m的重物从高处放下,如图所示,若重物以加速度α下降,则人对地面的压力为( )
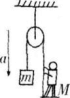
- A (M十,m)g-ma
- B M(g-d)-ma
- C (M-m)g+ma
- D Mg-ma
- 参考答案:C
- 您的答案:
参考解析:
本题考查了受力分析的知识点。
对重物受力分析可得绳的张力F=mg-ma,对人受力分析可得人对地面的压力为N=M9-F,两式联立得N=(M-m)g-ma。
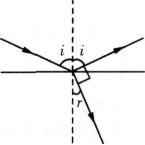
光从甲介质射入乙介质,由图可知( )
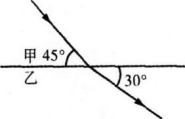
- A 甲介质是光疏介质,乙是光密介质
- B 入射角大于折射角
- C 光在甲介质中的传播速度较大
- D <img src='http://tp.mxqe.com/data/878/20178396_0_1.png' alt='物理化学综合,押题密卷,2022年成人高等考试《理化综合》(高升本)押题密卷' title='物理化学综合,押题密卷,2022年成人高等考试《理化综合》(高升本)押题密卷'>
- 参考答案:D
- 您的答案:
参考解析:
本题考查了光的折射的知识点。
入射角为i=45。,折射角为r=60。,可判断甲为光密介质,乙为光疏介质,则光在甲介质中的传播速度较小;若乙为空气,则甲的折
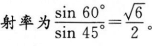
在垂直于纸面向里的匀强磁场中有一正三角形通电导体线框,线框平面跟磁场方向垂奁.电流方向如图所示,则( )
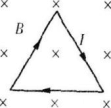
- A 线框每边所受磁场的作用力指向线框内部,合力为零
- B 线框每边所受磁场的作用力指向线框内部,合力不为零
- C 线框每边所受磁场的作用力指向线框外部,合力为零
- D 线框每边所受磁场的作用力指向线框外部,合力不为零
- 参考答案:C
- 您的答案:
参考解析:
本题考查了左手定则、受力分析的知识点。
由左手定则可判断,线框每边受到的磁场的作用力指向线框外部且大小相等,由受力分析可得舍力为零。
根据电容器电容的定义式C—Q/U,可知,以下说法正确的是( )
- A 电容器带电的电量越多,它的电容就越大,电容与电量成正比
- B 电容器不带电时,其电容为零
- C 电容器两极间的电压越高,它的电容就越小,电容与电压成反比
- D 电容器的电容大小与电容器的Q、U值无关
- 参考答案:D
- 您的答案:
参考解析:
本题考查了电容器电容的决定因素的知识点。
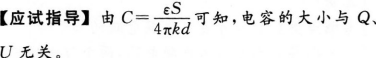
如图所示,一矩形线圈长为a,宽为b,线圈电阻为R。从磁感应强度为B的匀强磁场中以速度v匀速拉出来,其产生的感应电动势和矩形线圈中的电流大小为( )
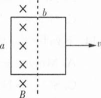
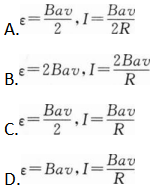
- A 见图A
- B 见图B
- C 见图C
- D 见图D
- 参考答案:D
- 您的答案:
参考解析:
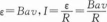
维修电炉时,将电炉丝的长度缩短十分之一,则修理前电炉的功率与维修后的功率之比为( )
- A 9∶10
- B 10∶9
- C 10∶11
- D 11∶10
- 参考答案:A
- 您的答案:
参考解析:
本题考查了电功率计算的知识点。
设维修前电炉丝的电阻为R,则

在斜面上放一物体静止不动,该物体受重力G、弹力N和静摩擦力厂的作用,该物体的受力图画得正确的是( )
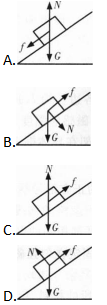
- A 见图A
- B 见图B
- C 见图C
- D 见图D
- 参考答案:D
- 您的答案:
参考解析:
本题考查了受力分析的知识点。
由弹力的性质可知,N的方向应为垂直于斜面向上,可知D正确。
伦琴射线实际上是( )
- A 电磁波
- B 高速电子流
- C 高速中子流
- D 高速质子流
- 参考答案:A
- 您的答案:
参考解析:
本题考查了光的电磁本性的知识点。
X射线是电磁波。
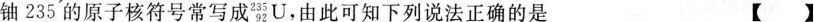
- A 铀235的原子核中有92个质子
- B 铀235的原子核中有92个电子
- C 铀235的原子核中有92个中子
- D 铀235的原子核中有235个中子
- 参考答案:A
- 您的答案:
参考解析:
本题考查了原子核的组成的知识点。
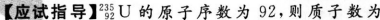
92,中子数为235-92=143。原子核内无电子。
实验室中用二氧化锰和浓盐酸制取氯气的反应中,得到的氯气恰能与标准状况下22.4升氢气完全反应,则被氧化的氯化氢的物质的量是( )
- A 4mol
- B 3mol
- C 2mol
- D 1mol
- 参考答案:C
- 您的答案:
参考解析:
本题考查了氧化还原反应中物质的量的计算的知识点。

n摩尔C2H4和n摩尔CO相比较,下列叙述不正确的是( )
- A 在同温同压下体积相等
- B 在同温同压下密度相等
- C 分子数相等
- D 在标准状况下质量不相等
- 参考答案:B
- 您的答案:
参考解析:
本题考查了气体物质的量的计算的知识点。
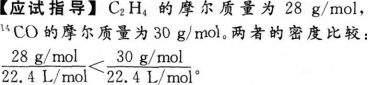
下列说法中,正确的是( )
- A 升高温度,原来的饱和溶液一定不再饱和
- B 恒温下,向NaCl的不饱和溶液中加入少量NaCl,则NaCl的溶解度增大
- C 把5gNaCl溶于100g水中,可制得5%NaCl溶液
- D 把25℃含有少量未溶KNO3的饱和溶液加热到80℃变成不饱和溶液,溶液的浓度增大
- 参考答案:D
- 您的答案:
参考解析:
本题考查了溶液的溶解度及浓度的知识点。
KN0。的溶解度随温度的升高而增大。当25℃(含有少量未溶)KN0。饱和溶液加热到80℃后虽然变成了不饱和溶液,溶解于其中的溶质的质量增多,溶液浓度增大。
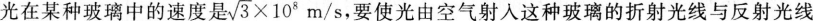
之间成90°角,则入射角是( )
- A 30
- B 45
- C 600
- D 90。
- 参考答案:C
- 您的答案:
参考解析:
本题考查了光的折射的知识点。
玻璃的折射率
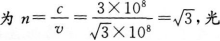
由空气射入这种玻璃的光路
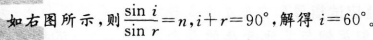
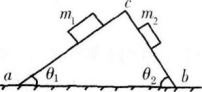
在粗糙水平面上有~个截面为三角形的木块abc,在它的两个斜面上分别放上两个质量为m和m2的物体,如图所示,已知abc和m1、m2都是静止的,则水平面对木块abc( )
- A 有摩擦力.其方向向左
- B 有摩擦力,其方向向右
- C 有摩擦力,其方向不能确定,因θ1、θ2、m1、m2的数据未给出
- D 没有摩擦力
- 参考答案:D
- 您的答案:
参考解析:
本题考查了物体的受力分析的知识点。
两个物体和木块可看成一个整体,整体只受到重力和支持力,没有摩擦力。
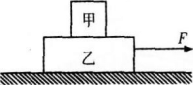
如图,甲乙两物体叠放于水平地面上,用水平力F拉物体乙,它们仍保持静止状态,甲乙两物体的接触面也为水平面,则乙物体的受力个数为( )
- A 3个
- B 4个
- C 5个
- D 6个
- 参考答案:C
- 您的答案:
参考解析:
本题考查了物体的受力分析的知识点。
对乙受力分析,如右图所示,则受力个数为5个。
如图,教室里同一块小黑板用相同的细绳按四种方式悬挂着,其中α<β,则细绳中的拉力,数值最大的是( )
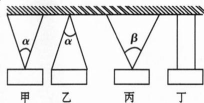
- A 甲图
- B 乙图
- C 丙图
- D 丁图
- 参考答案:C
- 您的答案:
参考解析:
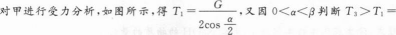
T2>T4,C正确。
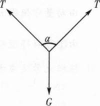
平行板电容器的两金属板带等量异种电荷,要使两板间的电压加倍,而板间的电场强度减半,采取的措施有( )
- A 两极板的电量加倍,而距离变为原来的4倍
- B 两极板的电量加倍,而距离变为原来的2倍
- C 两极板的电量减半,而距离变为原来的4倍
- D 两极板的电量减半,而距离变为原来的2倍
- 参考答案:C
- 您的答案:
参考解析:
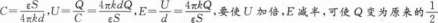
.d变为原来
的4倍,C正确。
一辆汽车从拱形桥桥顶开始匀速驶下的过程中,以下说法正确的是( )
- A 动能变化等于势能变化
- B 它的机械能守恒
- C 它所受合外力为零
- D 它所受外力做功的代数和为零
- 参考答案:D
- 您的答案:
参考解析:
本题考查了机械能守恒定律、动能定律的知识点。
汽车匀速驶下时,动能不变,势能减小,合外力做功为零,它所受外力不为零。
影响化学反应速率的因素很多,下列措施一定能使2H2O2==2H2O+O2十反应速率加快的是
( )
- A 降低温度
- B 升高温度
- C 降低反应物浓度
- D 减小压强
- 参考答案:B
- 您的答案:
参考解析:
本题考查了影响化学反应速率的因素的知识点。
根据影响化学反应速率的因素,升高温度、增大压强,增大反应物的浓度、加催化剂等都能使反应速率加快。
下列各组液体混合物不能用分液的方法分离的是( )
- A 苯和水
- B 正己烷和水
- C 乙酸乙酯和水
- D 乙醇和水
- 参考答案:D
- 您的答案:
参考解析:
本题考查了有机物的水溶性的知识点。
两种互不相溶的液体,可用分液法将它们分离,而乙醇和水能互溶。
X、Y、Z三种金属,Y在金属活动性顺序表中位于氢元素之后。X与Fe组成的原电池中,X是负极。将Y、Z两种金属分别投入盛有硫酸铜溶液的试管中,过一段时间,金属Y表面附有金属铜,Z的表面没有变化,则这三种金属的活动性顺序是( )
- A X>Y>Z
- B X>Z>Y
- C Y>X>Z
- D 无法比较
- 参考答案:A
- 您的答案:
参考解析:
本题考查了金属活动性顺序及原电池原理的知识点。
根据题意X与Fe组成原电池,X是负极说明金属活动性X>Fe。由于Y、Z两种金属分别投入盛有CuSO4溶液的试管,Y表面有Cu说明Y的金属性大于Cu,而Z表面无变化,说明Z金属性小于Cu,所以金属活动性Y>Z,又因Y的金属活动性在H之后,所以金属活动性X>Y>Z。
把Zn粒加入0.1mol/L盐酸中,若要加快产生H2的速率,可采取的方法是( )
- A 加入少量NaOH溶液
- B 加入ZnO
- C 滴加少量CuSO4溶液
- D 滴加MgCl2溶液
- 参考答案:C
- 您的答案:
参考解析:
本题考查了影响化学反应的因素的知识点。
滴加少量CuSO4溶液后,则发生反应:Zn+CuSO4==ZnSO4+Cu,形成铜、锌原电池,放出H2的速率会更快。
既能与盐酸反应,又能与氢氧化钠溶液反应的单质是( )
- A S
- B Fe
- C C
- D Al
- 参考答案:D
- 您的答案:
参考解析:
本题考查了物质的化学性质的知识点。
根据所给选项,既能与盐酸反应又能与NaOH溶液反应的“单质”只有Al单质。
在相同条件下,aL氢气和bL氨气所含原子数相同,则a与b之比为( )
- A 1∶1
- B 2∶1
- C 1∶2
- D 1∶3
- 参考答案:B
- 您的答案:
参考解析:
本题考查了同温同压下气体的体积与物质的量和粒子数目的换算的知识点。
1个氢分子H2中舍2个H原子,1个氨分子NH。中含4个原子,根据阿伏加德罗定律,2a=4b,所以a∶b=2:1。
下列物质存在同分异构体的是( )
- A CH3CH3
- B CH4
- C CH3CH2CH2CH3
- D CH3CH2CH3
- 参考答案:C
- 您的答案:
参考解析:
本题考查了同分异构体的知识点。
同分异构体指具有相同的分子式,但具有不同结构的化合物。根据题给4种物质,只有C项中物质有同分异构体。
一束橙色光与界面成30。角由空气射人某介质,折射角为30。,则此介质对橙色光的折射率为______,橙色光在此介质中的传播速度为______m/s。
在酸或碱存在的条件下,甲酸甲酯跟水发生水解反应的化学方程式为_______。
碳酸氢钠溶液和烧碱溶液反应的离子方程式为_______。
一小物块以速度v0=10m/s沿光滑地面滑行,然后沿光滑曲面上升到顶部水平的高台上,并由高台上飞出,如图所示。问当高台的高度h多大时,小物块飞行的水平距离最大这个距离是多少(g=10m/s2)

- 参考答案:
- 您的答案:
参考解析:
本题考查了机械能守恒定律、平抛运动的规律的知识点。
物块上滑至高处平台的过程,设其到平台处的速度为v1,由机械能守恒定律可得

由数学知识知:当h=2.5m时,小物块飞行的水平距离最大。将h=2.5m代入上式得此时的水平距离为5m.
固定在匀强磁场中的正方形导线框abcd,各边长为1.其中ab是一段电阻为R的均匀电阻丝,其余3边均为电阻可忽略的铜线。磁场的磁感应强度为B,方向垂直纸面向里。现有一与ab段的材料、粗细、长度都相同的电阻丝PQ架在导体框上,如图所示。PQ以恒定速度方向如何
把10gMgCl2和MgSO4的混合物溶于适量水中,滴加2mol/L的BaCl2溶液至沉淀完全,共消耗BaCl2溶液25mL。求混合物中MgCl2和MgSO4的质量各是多少克
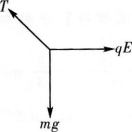
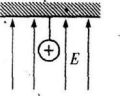
用一根轻绝缘细线悬挂一个质量为m、带电量为q的带正电的小球,如右图所示,空间有竖直向上的匀强电场,小球在静止时绳的拉力为mg/3,那么电场强度的大小为_______。若电场强度的大小不变,方向改为水平向右;则当小球静止时绳的拉力为_______。
500mLNa2SO4溶液中含有0.2mol的Na+,则Na2sO4溶液的物质的量浓度为_______。
B.M.Trostl991年提出了原子经济的概念:若所有反应物均全部转化为欲得的产物,则此反应就是100%的原子经济反应。对于加成、取代和消去三种反应类型而言,其中最具有原子经济反应潜力的应是_______反应。
- 参考答案:
- 您的答案:
参考解析:
加成
加成、取代、消去三种反应,其中取代和消去反应之可逆程度远大于加成反应。而加成反应的过程则是分子由不饱和向饱和逐渐转化的过程.是稳定性增加的过程,其可逆程度较低,故最具有原子经济反应潜力。

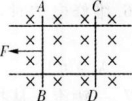
如右图所示的两条导轨水平放置在同一水平面上(即纸面上),磁场方向垂直向下(即垂直纸面向里),最初静止的导体AB、CD可以在导轨上自由滑动。当AB在外力作用下向左运动时,CD将向_______运动。磁场对AB的作用力的方向向_______,磁场对CD的作用力的方向向_______。
为了测定变压器的原、副线圈的匝数,可以在变压器的闭合铁芯上再临时绕一个线圈,已知临时绕的线圈是5匝,将变压器的原线圈接到电压是220V的交流电源上,测得副线圈和临时绕的线圈两端的电压分别是6.0V和0.40V。由此可知这个变压器的原线圈的匝数是_______匝;副线圈的匝数是_______匝。
- 参考答案:
- 您的答案:
参考解析:
275075
本题考查了变压器电压与匝数的关系的知识点。
n1:n2:n3=U1:U2:U3,即n1:n2:5=220:6.0:0.40,可得n1=2750,n2=75。
浓硝酸常盛装在棕色瓶中,且贮放在冷暗处,原因是____________________________,
在反应3Cu+8HNO3==3Cu(NO3)2+2NO↑+4H2O中,HNO3所表现的性质_____________________
- 参考答案:
- 您的答案:
参考解析:
浓HNO3不稳定,见光受热易分解强氧化性和酸性
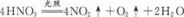
(硝酸浓度越大,越易分解)。硝酸是一种强酸,除具有酸的通
性外,还具强氧化性,Cu与HNO3反应中的产物中Cu(NO3)2反映硝酸的酸性,NO反映硝酸的强氧化性。
通常情况下,钠在空气中燃烧火焰呈黄色;氢气在氯气中燃烧火焰呈_______色;甲烷在空气中燃烧火焰呈_______色。
欲除去乙烷中的乙烯,可将混合气体通过盛有_______的洗气瓶;欲除去乙炔中的硫化氢,可将混合气体通过盛有_______的洗气瓶。
- 参考答案:
- 您的答案:
参考解析:
溴水NaOH溶液(或CuSO4溶液)
由于乙烯能与Br2发生加成反应,而乙烷不能,故可以通过盛有溴水的洗气瓶,将乙烷中的乙烯除去。由于NaOH溶液能与H2S气体反应:2NaOH+H2S==Na2S+2H2O(或CuSO4+H2S==CuS↓+H2SO4),故能将乙炔中混有的H2S除去。
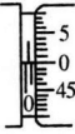
如图所示,螺旋测微器测出的金属丝的直径是______。
用伏安法测量电源的电动势和内阻,测得U1=l.10V,I1=0.10A,U2=0.30V,I2=0.60A,则电源电动势E=_______V,内阻r=_______Ω。
从距地面高为h1=l.25m处竖直向下抛出皮球,碰地后皮球跳起的高度h2=2.5m,不计空气阻力,设球碰撞地面时无机械能损失(g取10m/s+++2),则皮球下抛时的初速度大小是________m/s。
若甲物体的质量是乙物体质量的2倍,现在把甲、乙两个物体以相同的初动能竖直向上抛出,不计空气阻力。则甲、乙两个物体上升的最大高度之比h甲:h乙=_______;甲、乙两个物体的最大重力势能之比E甲:E乙=_______。
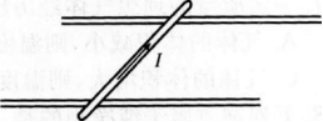
如右图所示,质量为1kg的金属杆静止于相距1m的两水平轨道上,金属杆中通有方向如右图所示的、大小为50A的恒定电流,两轨道间存在竖直方向的匀强磁场。金属与轨道间的动摩擦因数为0.6,欲使杆向右匀速运动,两轨道间磁场方向应为_______,磁感应强度8的大小应为_______T。(9=10m/s2)
甲、乙两车从同一地点同时出发,甲以速度v0。做匀速运动,乙从静止开始做匀加速运动,则乙追上甲时乙的速度为_______,乙追上甲之前,甲乙之间距离最大时乙的速度为_______。
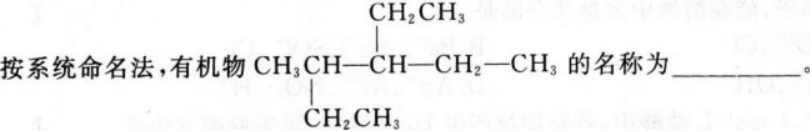
- 参考答案:
- 您的答案:
参考解析:
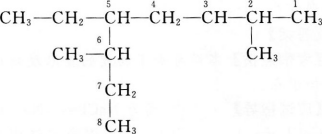
本题考查了烷烃的系统命名的知识点。
根据有机物的命名方法:先找主链(碳原子数最多的链)可知该有机物的主链中含有6个碳原子;根据编号原则确定取代基的位置,先从取代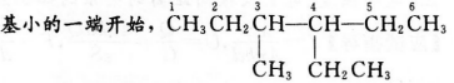
因此本题所示结构的名称为3-甲基-4-乙基己烷。
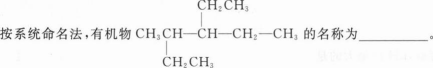
- 参考答案:
- 您的答案:
参考解析:
3-甲基-4-乙基己烷
根据有机物的命名方法:先找主链(碳原子数最多的链)可知该有机物的主链中含有6个碳原子;根据编号原则确定取代基的位置,先从取代基小的一端开始,
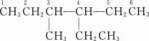
因此本题所示结构的名称为3-甲基-4-乙基己烷。
质量相等的Li、Na、K三种金属分别加入足量的水中完全反应,在相同条件下所得H2的体积比为________。.
要除去硫酸亚铁溶液中含有的少量Fe3+和Cu2+抖,最好加入的试剂是_______。
有下列几种气体:H2、O2、HCl、NO、NH3、CH4,其中通常情况下能用来和水做“喷泉”实验的是_______。
- 参考答案:
- 您的答案:
参考解析:
本题考查了气体的水溶性的知识点。
氯化氢气体和氨气,在常温下都极易溶解于水(0℃时,1体积水约能溶解500体积的氯化氢;通常状况下,1体积水约能溶解700体积的氨气)。
常温下呈液态的非金属单质是________(填分子式),地壳中含量最多的非金属元素是氧。
氢硫酸在空气中长时间放置以后,变浑浊的原因用化学方程式表示为_______。
- 参考答案:
- 您的答案:
参考解析:
本题考查了氢卤酸的化学性质的知识点。
氢硫酸的还原性比H2S气体的还原性更强。它更容易被氧化。硫化氢水溶液在空气中放久了会变浑浊,就是被空气氧化析出硫所致。
完全燃烧0.1mol某烯烃X,生成0.2mol二氧化碳。在一定条件下,X跟氯化氢反应生成Y。X为_______;Y为_______。
- 参考答案:
- 您的答案:
参考解析:
乙烯氯乙烷
本题考查了确定物质的化学式的知识点。
由于烯烃的通式为cnH2n,已知0.1摩烯烃能生成0.2摩CO2,则说明n=2,是乙烯。乙烯可与氯化氢发生加成反应:
CH2=CH2+HCl→CH3-CH2Cl
明矾水解所产生的_______吸附能力很强,可吸附悬浮杂质,使水澄清。
- 参考答案:
- 您的答案:
参考解析:
AI(OH)3胶体
本题考查了水的净化的知识点。
明矾是指含12个结晶水的硫酸铝钾KAl(S04)2·12H2O。由于其水解形成的胶体Al(OH)3具有较强的吸附能力,所以明矾可作净水剂。
写出下列化学反应的离子方程式并配平:
FeS和稀硫酸反应制取硫化氢气体:____________________________。
在CO、SO2、Cl3、CO2、NO2几种气体中,无色无味且有毒的气体和可造成“温室效应”的气体分别是________。
乙醇跟氢卤酸反应生成卤代烃和水的化学方程式为_______。
某晶体盐的水溶液呈浅绿色,在此溶液中通入氯气,溶液变为棕黄色,把所得棕黄色溶液分成两份:一份加入KSCN溶液,溶液变深红色;另一份加入BaCl2溶液,产生不溶于稀HNO3的白色沉淀,则该晶体盐的化学式是_______。
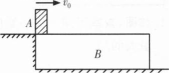
如图所示,光滑水平地面上的长木板B,其质量M=8kg,质量为m=2kg的小物块A以v0=10m/s的初速度滑上木板B,已知A、B间动摩擦因数μ=0.4,求:小物块A的最终速度及A在B上滑行的距离。(设B足够长,取g=10m/s2)
如图所示,金属杆a从高为h处从静止开始沿弧形轨道下滑。导轨平行的水平部分有竖直向下的匀强磁场B,水平部分导轨上原来放有一长L的金属杆b。已知a杆的质量m1,且与b杆的质量之比m1。m2=3:4,水平导轨足够长。两棒始终没有相碰,不计摩擦。求:a和b的最终速度分别是多大?
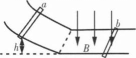
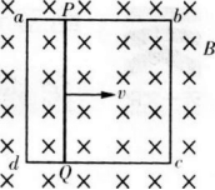
固定在匀强磁场中的正方形导线框abcd,各边长为ι,其中ab是一段电阻为R的均匀电阻丝,其余3边均为电阻可忽略的铜线。磁场的磁感应强度为B,方向垂直纸面向里。现有一与ab段的材料、粗细、长度都相同的电阻丝PQ架在导体框上,如图所示。PQ以恒定速度v从ad滑向bc,当滑过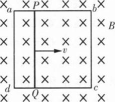 的距离时,通过PQ段电阻丝的电流强度是多大?方向如何?
的距离时,通过PQ段电阻丝的电流强度是多大?方向如何?

1.15g金属钠跟水反应后,得到100mL溶液,试计算:
(1)生成的气体在标准状况下是多少毫升?
(2)反应后所得溶液的物质的量浓度是多少?