若要除去硫酸亚铁中含有的少量Fe3+和Cu2+,最好加入.
正确答案及解析
正确答案
解析
铁粉 【解题指要】除杂质有以下要求:
(1)把杂质除去或使其变成能与所需要的有效成分分离开的物质.如此题为除去FeSO4中
的Fe3+和Cu2+,加入铁粉后发生如下反应:

第一个反应把杂质(Fe3+)变成了有效成分(Fe2+),这种结果最好.第二个反应把混在溶液中
的Cu2+变成了不溶于水的Cu单质,用过滤法即可与Fe2+分开.
(2)不能引入新杂质.只从与Fe3+、Cu2+反应的角度看,不加铁粉加锌粉也可以.因为加锌粉
后,发生如下反应:
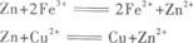
从反应方程式看,的确除去了Fe3+和Cu2+,但却引入了Zn2+,不符合要求.